气体净化的几种方法: (1)吸收法:用吸收剂将杂质气体吸收除去。如除去CO中混有的少量CO
2,可先用浓NaOH溶液吸收CO
2,再用浓硫酸等干燥剂除去水蒸气。常用吸收剂如下表:
| 吸收剂 |
吸收的气体杂质 |
吸收剂 |
吸收的气体杂质 |
| 水 |
可溶性的气体:HCl,NH3 |
NaOH |
CO2,HCl,H2O |
| 无水CuSO4 |
H2O |
碱石灰 |
CO2,HCl ,H2O |
| 灼热的铜网 |
O2 |
NaOH |
CO2,HCl |
| 灼热的CuO |
H2,CO |
浓硫酸 |
H2O |
(2)转化法:通过化学反血,将杂质气体转化为所要得到的气体:如除去CO
2中的CO,可将混合气体通过足量的灼热CuO+CO

Cu+CO
2
气体的干燥:
气体的干燥是通过干燥剂来实现的,选择干燥剂要根据气体的性质。一般原则是:酸性干燥剂不能用来干燥碱性气体,碱性干燥剂不能用来干燥酸性气体,干燥装置由干燥剂的状念决定.
(1)常见的干燥剂
| 干燥剂 |
可干燥的气体 |
不可干燥的气体 |
| 名称或化学式 |
酸碱性 |
状态 |
| 浓H2SO4 |
酸性 |
液体 |
H2、N2、O2、CO2、HCl、CH4、CO |
NH3 |
| 固体NaOH、生石灰,碱石灰(氢氧化钠和生石灰的混合物) |
碱性 |
固态 |
H2、O2、N2、CH4、CO、NH3等 |
CO2、SO2、HCl |
| 无水CaCl2 |
中性 |
固态 |
除NH3外的所有气体 |
NH3 |
(2)干燥装置的选择
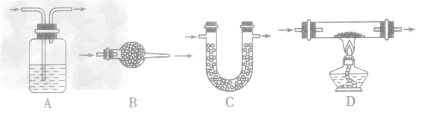
①除杂试剂为液体时,常选用洗气瓶,气体一般是 “长进短出”,如下图A。
②除杂试剂为同体时,常选用干燥管(球形或u 形),气体一般是“大进小出”,如下图B、C。
③需要通过加热与固体试剂发生化学反应除去的气体,常采用硬质玻璃管和酒精灯,如下图D。
 装置连接顺序的确定规律:
装置连接顺序的确定规律: (1)除杂和干燥的先后顺序
①若用洗气装置除杂,一般除杂在前,干燥在后。原因:从溶液中出来的气体通常混有水蒸气,干燥在后可将水蒸气完全除去。如除去CO中混有的CO
2和水蒸气,应将气体先通过。NaOH溶液,再通过浓H
2SO
4。
②若用加热装置除杂,一般是干燥在前,除杂在后。如除去CO
2中混有的CO和水蒸气,应将气体先通过浓H
2SO
4,再通过灼热的CuO。
(2)除去多种杂质气体的顺序一般是先除去酸性较强的气体。如N2中混有 HCl、H
2O(气)、O
2时,应先除去HCl,再除去水,最后除去O
2(用灼热的铜网)。
(3)检验多种气体的先后顺序(一般先验水蒸气):有多种气体需要检验时,应尽量避免前步检验对后步检验的干扰。如被检验的气体中含有CO
2和水蒸气时,应先通过无水CuSO
4。检验水蒸气,再通过澄清的石灰水检验CO
2.
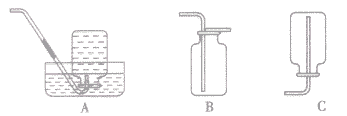
确定气体收集方法的技巧: (1)排水集气法适用于“不溶于水且小与水反应的气体”,如下图A。
(2)向上排空气法适用于“密度比空气大且小与空气成分反应的气体”(相对分子质量大于29的气体),如下图B。
(3)向下排空气法适用于“密度比空气小且小与空气成分反应的气体”(相对分子质量小于29的气体),如下图C。
(4)不能用排空气法收集的气体
①气体的密度与空气的密度相近时不能用排空气法收集
②当气体与空气中某一成分反应时不能用排空气法收集
(5)有毒气体收集方法的确定
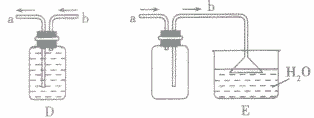
①有毒,但气体难溶于水时,一般采用排水法收集。如下图D
②有毒,但气体叉易溶于水时,则采用带双孔胶塞(一长一短的导气管)的集气瓶利用排空气法收集该气体,但必须接尾气处理装置,以免多余的有毒气体逸散到空气中污染空气,如收集氨气可用图E。
 气体制取实验中关于仪器或装置选择题目的解题技巧:
气体制取实验中关于仪器或装置选择题目的解题技巧: (1)需要研究气体实验室制法的化学反应原理;
(2)需要研究制取这种气体所应采用的实验装置;
(3)需要研究如何证明制得的气体就是要制取的气体。
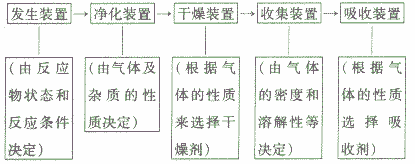
根据给出的仪器或装置进行选取时,应明确制取气体的发生装置主要是两套(同体加热型和固液常温型),依据反应物的状态和反应条件来确定选用哪套发生装置;气体的收集装置主要就是三套(向上排空气法、向下排空气法和排水法),依据气体的性质来确定选用什么样的收集装置。选择仪器时要注意先对实验原理进行判断,然后再根据原理确定装置所需要的仪器。






 ”的反应,简称“固体加热型”,装置如图A所示,如用KMnO4或KClO3和MnO2制O2。
”的反应,简称“固体加热型”,装置如图A所示,如用KMnO4或KClO3和MnO2制O2。  ”的反应,简称“固液常温型”,装置如图B、C、D、E。如用H2O2和MnO2制O2、用锌粒与稀H2SO4制H2或用CaCO3与稀盐酸制CO2。同B装置相比,D装置具有便于添加液体药品,制取的气体量较多的优点;C装置不仅添加液体药品方便,而且可通过导管上的开关控制反应的发生和停止;E装置可通过分液漏斗的活塞控制加入药品的量和速度。
”的反应,简称“固液常温型”,装置如图B、C、D、E。如用H2O2和MnO2制O2、用锌粒与稀H2SO4制H2或用CaCO3与稀盐酸制CO2。同B装置相比,D装置具有便于添加液体药品,制取的气体量较多的优点;C装置不仅添加液体药品方便,而且可通过导管上的开关控制反应的发生和停止;E装置可通过分液漏斗的活塞控制加入药品的量和速度。 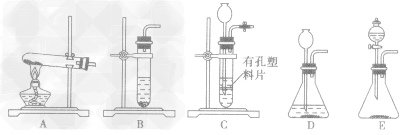
 ”的反应的发生装置的其他改进:
”的反应的发生装置的其他改进: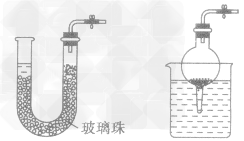



 Cu+CO2
Cu+CO2

