锌锰干电池是最早使用的化学电池,其基本构造如图所示.
(1)锌锰干电池的负极是______,电路中每通过0.2mole-,负极质量减少______g;工作时NH4+离子在正极放电产生两种气体,其中一种气体分子是含10e-的微粒,正极的电极反应式是______.
(2)某研究小组对电池内黑色糊状物进行了下列实验.
电池内黑色糊状物粉末
无色溶液
溶解过滤
黑色残渣
已知:Zn(OH)2是两性氢氧化物.完成下列实验报告.
| 实验步骤 |
实验现象 |
实验结论和解释 |
| 取少量上述无色溶液于试 管中,逐滴加入NaOH溶液,直至过量,再加热 |
生成白色沉淀,
______
______ |
无色溶液中存在Zn2+、NH4+离子
检验NH4+离子存在的离子方程式是
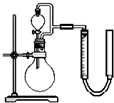
______ | (3)利用残渣中分离出的MnO2,研究其在H2O2制O2过程中的作用.实验装置如右图所示.将等物质的量浓度、等体积H2O2溶液加入烧瓶中,分别进行2个实验(气体的体积在相同条件下测定).
| 序号 |
烧瓶中的物质 |
实验记录 |
实验结论与解释 |
| 实验一 |
足量MnO2 |
收集到56mL气体 |
MnO2做催化剂 |
| 实验二 |
足量MnO2和稀硫酸 |
黑色粉末部分溶解,
收集到112mL气体 |
MnO2做氧化剂,生成Mn2+离子 | 实验一、二中参加反应的H2O2的物质的量之比为______,实验二中反应的离子方程式为______. |


