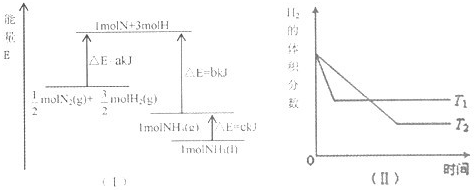
T℃时,N2与H2反应生成NH3,其能量变化如图(I)所示.若保持其他条件不变,温度分别为T1℃和T2℃时,H2的体积分数与时间的关系如图(Ⅱ)所示.则下列结论正确的是( )
A.该反应的热化学方程式是:
1/2N2(g)+3/2H2(g)?NH3(g)△H=-(a+b)kJ?mol-1
|
|
B.该反应的热化学方程式:N2(g)+3H2(g)?2NH3(l)△H=-2(b+c-a)kJ?mol-1
|
|
C.T1<T2,且正反应为放热反应
|
|
D.其他条件不变,升高温度,正、逆反应速率均增大,且H2的转化率增大
|
|

