在0.1 mol·L-1NH3·H2O溶液中存在如下电离平衡:NH3·H2O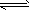 NH4+ + OH-。对于该平衡,下列叙述中正确的是 NH4+ + OH-。对于该平衡,下列叙述中正确的是 |
|
[ ] |
A.降低温度,溶液中c(NH4+)增大
B.加入少量NaOH固体,平衡向逆反应方向移动,电离平衡常数减小
C.加入少量0.1 mol·L-1HCl溶液,溶液中c(OH-)增大
D.加入水时,溶液中c(OH-)/c(NH3·H2O) 增大 |
根据n多题专家分析,试题“在0.1mol·L-1NH3·H2O溶液中存在如下电离平衡:NH3·H2ONH4++OH-。对于该平衡,下列叙述中正确的是[]A.降低温度,溶液中c(NH4+)增大B.加入少量NaOH固体,平衡向逆反应方向移动…”主要考查了你对 【弱电解质电离的影响因素】 等知识点的理解和应用能力。关于这些知识点的“档案”,你可以点击相应的链接进行查看和学习。
与“在0.1mol·L-1NH3·H2O溶液中存在如下电离平衡:NH3·H2ONH4++OH-。对于该平衡,下列叙述中正确的是[]A.降低温度,溶液中c(NH4+)增大B.加入少量NaOH固体,平衡向逆反应方向移动”考查相似的试题有:

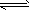 NH4+ + OH-。对于该平衡,下列叙述中正确的是
NH4+ + OH-。对于该平衡,下列叙述中正确的是