恒温下,将16 mol N2与24 mol H2的混合气体通入一个固定容积为4L的密闭容器中,发生如下反应:N2(g)+3H2(g)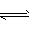 2NH3(g),10分钟后反应达平衡时,NH3的含量(体积分数)为25%,下列的关说法正确的是 2NH3(g),10分钟后反应达平衡时,NH3的含量(体积分数)为25%,下列的关说法正确的是 |
|
[ ] |
A.达到平衡时,N2和H2的转化率之比为1:1
B.10分钟内v(H2)=0.35mol/(L·min)
C.平衡混合气体的密度为128g/L
D.平衡混合气体中,n(N2):n(H2):n(NH3)=1:3:2 |
根据n多题专家分析,试题“恒温下,将16molN2与24molH2的混合气体通入一个固定容积为4L的密闭容器中,发生如下反应:N2(g)+3H2(g)2NH3(g),10分钟后反应达平衡时,NH3的含量(体积分数)为25%,下列的关说…”主要考查了你对 【化学平衡的有关计算】 等知识点的理解和应用能力。关于这些知识点的“档案”,你可以点击相应的链接进行查看和学习。
与“恒温下,将16molN2与24molH2的混合气体通入一个固定容积为4L的密闭容器中,发生如下反应:N2(g)+3H2(g)2NH3(g),10分钟后反应达平衡时,NH3的含量(体积分数)为25%,下列的关说”考查相似的试题有:

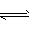 2NH3(g),10分钟后反应达平衡时,NH3的含量(体积分数)为25%,下列的关说法正确的是
2NH3(g),10分钟后反应达平衡时,NH3的含量(体积分数)为25%,下列的关说法正确的是