
| 下列化合物中属于弱电解质的是 |
|
[ ] |
| A.BaSO4 B.HCl C.CO2 D.H2O |
| 化学平衡主要研究下列哪一类反应的规律 |
|
[ ] |
| A.可逆反应 B.化合反应 C.离子反应 D.气体反应 |
| 有关化学反应的说法中,正确的是 |
|
[ ] |
| A.自发反应都是放热反应 B.自发反应都是熵增大的反应 C.能自发进行的吸热反应一定是熵增大的反应 D.非自发反应在任何条件下都不能实现 |
| 下列变化中属于吸热反应的是 |
|
[ ] |
| A.葡萄糖在人体内缓慢氧化 B.灼热的炭和二氧化碳气体化合 C.铝粉与氧化铁粉末反应 D.过氧化钠与水的反应 |
| 下列各式表示的变化中,熵变(△S)最大的是 |
|
[ ] |
| A.2H2O == 2H2 + O2 B.C2H5OH(l) == C2H5OH(s) C.Fe+S == FeS D.CO2 + 2NaOH == Na2CO3 + H2O |
| 下列电离方程式中正确的是 |
|
[ ] |
A.CaCO3 Ca2+ + CO32- Ca2+ + CO32- B.H2CO3  2H+ + CO32- 2H+ + CO32- C.NH3·H2O  NH3 + H2O NH3 + H2OD.H2SO3  H+ + HSO3- H+ + HSO3- |
在一定条件下,能说明可逆反应X(g)+Y(g) Z(g)+W(g)已经达到平衡状态的是 Z(g)+W(g)已经达到平衡状态的是 |
|
[ ] |
| A. 容器内压强不随时间的变化而变化 B. X、Y、Z、W的浓度比保持不变 C. X的消耗速率与Z的生成速率相等 D. c(X) · c(Y)=c(Z) · c(W) |
对于处于化学平衡状态的反应C(s) + H2O(g) CO(g) + H2(g) △H>0,既要提高反应速率又要提高H2O的转化率,下列措施中可行的是 CO(g) + H2(g) △H>0,既要提高反应速率又要提高H2O的转化率,下列措施中可行的是 |
|
[ ] |
| A.增大H2O(g)的浓度 B.降低压强 C.升温 D.使用合适的催化剂 |
| 根据以下3个热化学方程式,下列有关Q1、Q2、Q3三者关系的判断中正确的是 2H2S(g)+3O2(g)=2SO2(g)+2H2O(l) △H=―Q1 kJ/mol 2H2S(g)+O2(g)=2S(s)+2H2O(l) △H=―Q2 kJ/mol 2H2S(g)+O2(g)=2S(s)+2H2O(g) △H=―Q3 kJ/mol |
|
[ ] |
| A.Q1>Q2>Q3 B.Q1>Q3>Q2 C.Q3>Q2>Q1 D.Q2>Q1>Q3 |
在不同情况下测得A(g)+3B(g) 2C(g)+2D(g)的下列反应速率,其中反应速率最大的是 2C(g)+2D(g)的下列反应速率,其中反应速率最大的是 |
|
[ ] |
| A.υ(D)=0.4 mol·L-1·s-1 B.υ(C)=0.5 mol·L-1·s-1 C.υ(B)=0.6 mol·L-1·s-1 D.υ(A)=0.15 mol·L-1·s-1 |
| 实验表明,在一定条件下,乙烯和水的反应可表示为:C2H4(g) + H2O (g) = C2H5OH(g) ΔH=-45.8 kJ/mol 则下列说法中正确的是 |
|
[ ] |
| A.实验中,乙烯的用量不会影响该反应的反应焓变ΔH B.0.5 mol H2O(l) 完全反应放出的热量为22.9 kJ C.1 mol C2H5OH(g)具有的能量大于1 mol C2H4(g)和1 mol H2O(g)所具有的能量和 D.1 mol C2H4(g)和1 mol H2O(g)中化学键的总键能大于1 mol C2H5OH(g)中化学键的总键能 |
在0.1 mol·L-1NH3·H2O溶液中存在如下电离平衡:NH3·H2O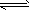 NH4+ + OH-。对于该平衡,下列叙述中正确的是 NH4+ + OH-。对于该平衡,下列叙述中正确的是 |
|
[ ] |
| A.降低温度,溶液中c(NH4+)增大 B.加入少量NaOH固体,平衡向逆反应方向移动,电离平衡常数减小 C.加入少量0.1 mol·L-1HCl溶液,溶液中c(OH-)增大 D.加入水时,溶液中c(OH-)/c(NH3·H2O) 增大 |
| 有关碰撞理论,下列说法中正确的是 |
|
[ ] |
| A.具有足够能量的分子(活化分子)相互碰撞就一定能发生化学反应 B.增大反应物浓度,可增大活化分子的百分数,从而使有效碰撞次数增大 C.升温能使化学反应速率增大,主要原因是增加了反应物分子中活化分子的百分数 D.催化剂不影响反应活化能,从而只影响反应速率不影响化学平衡 |
| 密闭容器中A与B反应生成C,其反应速率分别用v(A)、v(B)、v(C)表示。已知v(A)、v(B)、v(C)之间有以下关系2 v(B) = 3 v(A)、2 v(C) = v(A)。则此反应可表示为 |
|
[ ] |
| A.3A+2B=6C B.2A+3B=2C C.2A+3B=C D.3A+2B=2C |
将H2和Br2充入恒容密闭容器,恒温下发生反应H2(g)+Br2(g) 2HBr(g) △H<0。平衡时Br2(g)的转化率为a;若初始条件相同,在绝热条件下进行上述反应(反应体系与),平衡时Br2(g)的转化率为b。a与b的关系是 2HBr(g) △H<0。平衡时Br2(g)的转化率为a;若初始条件相同,在绝热条件下进行上述反应(反应体系与),平衡时Br2(g)的转化率为b。a与b的关系是 |
|
[ ] |
| A.a>b B.a=b C.a<b D.无法确定 |
| 实验测得碳单质、氢气、甲烷的燃烧热(△H)分别为-393.5 kJ/mol、-285.8 kJ/mol、-890.3 kJ/mol。则 CH4(g) == C(s) + 2H2(g)的反应焓变(△H)为 |
|
[ ] |
| A.-74.8 kJ/mol B.+74.8 kJ/mol C.-211kJ/mol D.+211kJ/mol |
密闭容器中充入2 mol SO2和1 mol O2发生反应:2SO2(g)+ O2(g) 2SO3(g) △H<0,并达到平衡状态。下列说法中,正确的是 2SO3(g) △H<0,并达到平衡状态。下列说法中,正确的是 |
|
[ ] |
| A.若容器体积不变,充入O2,平衡向右移动,SO3的百分含量一定增大 B.若容器体积不变,充入Ar,容器内压强增大,平衡向右移动 C.若容器压强不变,充入SO3(g),平衡向左移动,达到新平衡时c(SO2)增大 D.升高温度,平衡向左移动,平衡常数K减小 |
一定条件下,二氧化氮和四氧化二氮之间存在平衡:2NO2(g) N2O4(g) △H<0 在测定NO2的相对分子质量时,下列条件中测定结果误差最小的是 N2O4(g) △H<0 在测定NO2的相对分子质量时,下列条件中测定结果误差最小的是 |
|
[ ] |
| A.130℃ 3.03×105 Pa B.25℃ 1.01×105 Pa C.130℃ 5.05×104 Pa D.0℃ 5.05×104 Pa |
向容积为2 L的密闭容器中充入2 mol A和1 mol B,在一定条件下发生反应:2A(g)+B(g) 3C(g) 经 3C(g) 经2s达到平衡后,测得C气体的浓度为0.6 mol·L-1。下列说法中正确的是 |
|
[ ] |
| ①用物质A表示该反应的平均反应速率为0.2 mol·L-1·s-1 ②用物质B表示该反应的平均反应速率为0.2 mol·L-1·s-1 ③平衡时物质A与B的转化率相等 ④平衡时物质B的浓度为0.2 mol·L-1 ⑤其它条件不变,向容器中再加入1 molC气体,达到新平衡时,C的体积分数不变 A.①②③ B.①③⑤ C.②④⑤ D.①③④ |
对于可逆反应:2A(g)+B(g) 2C(g) △H<0,下列各图中正确的是 2C(g) △H<0,下列各图中正确的是 |
A.  B.  C.  D.  |
| 一定温度下,固定体积的容器中充入1 mol SO2和1 mol O2,再加入少量的NO,在体系中发生 ①2NO+O2=2NO2;②SO2+NO2=SO3+NO,下列说法中不正确的是 |
|
[ ] |
A.体系中的总反应是:2SO2+ O2 2SO3 2SO3 B.在反应过程中NO是催化剂 C.NO参与反应历程,降低反应活化能,加快反应速率 D.NO的引入可以增加SO2的平衡转化率 |
可逆反应aX+2Y(g) 2Z(g)在一定条件下的达到平衡后,t1和t2时各改变某一种外界条件,化学反应速率(v)-时间(t)图象如图。则下列说法中正确的是 2Z(g)在一定条件下的达到平衡后,t1和t2时各改变某一种外界条件,化学反应速率(v)-时间(t)图象如图。则下列说法中正确的是 |
 |
|
[ ] |
| A.若X是固体,则t1时一定是增大了容器的压强 B.若X是气体,则t2时可能是增大了容器的压强 C.若X是固体,则t1时可能是增大了X的质量 D.t2时不可能是减小容器压强;若采用了降温措施,则该反应的正反应方向△H<0 |
| 取c(H+)均为0.01 mol/L的盐酸和醋酸各100mL分别稀释2倍后,再分别加入0.03g锌粉,在相同条件下充分反应,有关叙述正确的是 |
|
[ ] |
| ① 醋酸与锌反应放出氢气多 ② 盐酸和醋酸分别与锌反应放出的氢气一样多 ③ 盐酸与锌反应放出氢气多 ④ 盐酸和醋酸分别与锌反应的速度一样大 ⑤ 醋酸与锌反应速率大 ⑥ 盐酸与锌反应速率大 A.①⑥ B.②⑤ C.③④ D.①⑤ |
一定温度下,在恒容密闭容器中发生如下反应:2A(g)+B(g) 3C(g),若反应开始时充入2mol A和2mol B,达平衡后A的体积分数为a%。其他条件不变时,若按下列四种配比作为起始物质,平衡后A的体积分数大于a%的是 3C(g),若反应开始时充入2mol A和2mol B,达平衡后A的体积分数为a%。其他条件不变时,若按下列四种配比作为起始物质,平衡后A的体积分数大于a%的是 |
|
[ ] |
| A.2mol C B.2mol A、3mol B和1mol He(He不参加反应) C.1mol B和1mol C D.2mol A、1mol B和3mol C |
| 工业上制备高纯硅反应的热化学方程式如下:SiCl4(g)+2H2(g)==Si(s)+4HCl(g) △H=+Q kJ/ mol(Q>0) 某温度、压强下,将一定量反应物通入密闭容器进行以上反应(此条件下为可逆反应),下列叙述中正确的是 |
|
[ ] |
| A.反应过程中,若增大压强能提高SiCl4的转化率 B.若反应开始时SiCl4为1 mol,则达平衡时,吸收热量为Q kJ C.反应至4 min时,若HCl浓度为0.12 mol/L,则H2的反应速率为0.03 mol/(L·min) D.当反应吸收热量为0.025Q kJ时,生成的HCl通入100 mL 1 mol/L的NaOH溶液恰好反应 |
| (1)CuCl2溶液有时呈黄色,有时呈绿色或蓝色,这是因为有CuCl2的水溶液中存在如下平衡: |
 |
| 现欲使溶液由黄色变成蓝色,请写出一种可采用的方法:_____________________。 (2)在2SO2+ O2  2SO3的平衡体系中,用由18O构成的氧气(18O2)替换掉一部分O2,平衡不发生移动。一段时间后SO2中18O的含量_________(填增加、减少或不变),其原因是__________。 2SO3的平衡体系中,用由18O构成的氧气(18O2)替换掉一部分O2,平衡不发生移动。一段时间后SO2中18O的含量_________(填增加、减少或不变),其原因是__________。(3)在恒温恒容的两个密闭容器A和B中,分别加入 a mol 和 b mol 的HI(a > b),发生反应: 2HI(g)  H2(g) + I2(g)达到平衡后。回答下列问题(用 “>”、“<” 或“=”填空): H2(g) + I2(g)达到平衡后。回答下列问题(用 “>”、“<” 或“=”填空):① 从反应开始到达到平衡所需要时间: tA _______ tB ② 平衡时的碘的浓度:cA(I2)______ cB(I2) ③ HI的平衡转化率:αA _______αB |
| (1)稀强酸、稀强碱反应生成1mol水时放出57.3 kJ的热。 ① 实验室中可用稀盐酸和氢氧化钡稀溶液反应来测定中和热。请写出能表示该反应中和热的热化学方程式_________________; ② 分别取100 mL 0.50 mol/L盐酸与100 mL 0.55 mol/L NaOH溶液进行中和反应。通过测定反应过程中所放出的热量可计算中和热。假设盐酸和氢氧化钠溶液的密度都是1g/cm3,中和后生成溶液的比热容c= 4.18 J/(g·℃)。实验时,测得反应前盐酸与NaOH溶液的平均温度为21.5℃,反应后混合溶液的温度为24.9℃。则实验测得的中和热△H=_______(保留1位小数) ③ 如果用含1 mol CH3COOH的稀醋酸与足量稀氢氧化钠溶液反应,反应放出的热____57.3 kJ(填“大于”、“小于”或“等于”);理由是_____________________________; (2)在催化剂的作用下CH4还原NO可以得到三种产物(该条件下均为气体),利用此反应能消除环境污染物NO。理论上每消耗标况下22.4 L NO就能放出290 kJ的热。写出该反应的热化学方程式 _____________________。 |
I、II为两个极易导热的密闭容器,I保持容积不变,II中的活塞可上下移动,以保持内外压强相等。在相同条件下将3 mol A和1 mol B分别同时混合充入I、II两容器中,发生反应3A(g)+B(g) 2C(g)+D(g) 2C(g)+D(g) (1)达到平衡时,I中A的浓度为M mol/L,C的浓度为N mol/L,II中A的浓度为m mol/L,C的浓度为n mol/L,则M_____m;N_____n;(填>、<、=) (2)保持温度不变,若向I中的平衡体系中再充入2 mol C和1 mol D,重新达到平衡后A的浓度为R mol/L。则_________ A. R = 2M B. R < M C. M < R < 2M D. R > 2M |
在100℃和200kPa的条件下,反应aA(g) bB(g)+cC(g)建立平衡后,在不加入任何物质的条件下逐步压缩体系的体积,增大体系的压强(维护温度不变),下表列出的不同压强下反应建立平衡时物质B的浓度。 bB(g)+cC(g)建立平衡后,在不加入任何物质的条件下逐步压缩体系的体积,增大体系的压强(维护温度不变),下表列出的不同压强下反应建立平衡时物质B的浓度。 |
 |
| 根据表中的数据,回答下列问题: (1)压强从200kPa增加到500kPa时,平衡_______移动(填“正向”或“逆向”或“不”),理由是 _________________。 (2)压强从500kPa增加到1000kPa时,平衡______移动(填“正向”或“逆向”或“不”),其原因可能为________________。 |
| 某学习小组通过测定大理石与硝酸反应过程中体系质量的变化,研究影响反应速率的因素。所用HNO3浓度为1.00 mol/L、2.00 mol/L,大理石有细颗粒与粗颗粒两种规格,实验温度为298 K、308 K,每次实验 HNO3的用量均为25.0 mL、大理石用量均为10.00g。 (1)请完成以下实验设计 |
 |
| (2)实验①中CO2质量随时间变化的关系见下图 |
 |
| 忽略溶液体积变化,计算实验①在40s-100 s范围内HNO3的平均反应速率(保留2位小数):_________________。 (3)画出实验②和③中CO2质量随时间变化关系的预期结果示意图。 |
 |
已知,常温下1体积水能溶解2体积氯气,并且氯水中有如下平衡:Cl2 + H2O HCl + HClO HCl + HClO (1)常温下,在一个体积为100mL的透明玻璃针筒里吸入80mL氯气后,再吸进10mL水,振荡后静置。写出针筒中观察到的现象是_____________________。 (2)将上述针筒长时间放置,又能看到何种变化__________;试用平衡观点加以解释__________。 |
在容积为2.0 L的密闭容器中充入0.60 mol X和1.60 mol Y,发生反应:aX(g)+3Y(g) 2Z(g) 经过10 min反应达到平衡状态,Y的浓度为0.2 mol/L,Z的物质的量分数为。计算并回答: 2Z(g) 经过10 min反应达到平衡状态,Y的浓度为0.2 mol/L,Z的物质的量分数为。计算并回答:① 10分钟内,Z的平均反应速率为 _______________ ② 计算a 的值(要求有具体过程)_____________ ③ 该条件下X的平衡转化率_____________________(百分数表示,保留一位小数) ④ 该条件下反应2Z(g)  aX(g)+3Y(g)的平衡常数为___________ aX(g)+3Y(g)的平衡常数为___________ ⑤ 将体积比为 1︰3的X和Y的混合气体,通入上述密闭容器中,在一定的条件下发生反应,达到化学平衡时,混合气体中A 的体积分数为w %(w < 25), 则混合气体中Z的体积分数是________,容器内的压强为反应前的_________ 倍。 |
| 科学家一直致力于研究常温、常压下“人工固氮”的新方法。曾有报道:在常温、常压、光照条件下, N2在催化剂(掺有少量Fe2O3的TiO2)表面与水发生反应,生成的主要产物为NH3和另一种常见气体。进一步研究NH3生成量与温度的关系(其它条件均相同),部分实验数据见下表 |
 |
| 回答下列问题: (1)写出该反应的化学方程式_____________________ (2)该反应的焓变△H______0(填“>”、“<”或“=”) (3)请在坐标图中画出上述反应在有催化剂与无催化剂两种情况下反应过程中体系能量变化示意图,并进行必要标注。 |
 |
| (4)与目前广泛使用的工业合成氨方法相比,该方法中固氮反应速率慢。请提出可提高其反应速率且增大NH3生成量的建议:___________________。 (5)已知: N2(g) + 3H2(g) == 2NH3(g) △H = -92.4 kJ/mol H2(g) + Cl2(g) == 2HCl(g) △H = -184.6 kJ/mol 1/2N2(g) + 2H2(g) + 1/2Cl2(g) == NH4Cl(s) △H = -313.6 kJ/mol ① 计算NH3(g) + HCl(g) == NH4Cl(s)的反应焓变:△H =______________ ② 室温下NH3就和HCl能发生化合反应生成NH4Cl;而在加热的条件下,NH4Cl则能分解为NH3和HCl。请用所学的化学原理解释这一现象:____________________________ |
| 在一定温度下,向一个容积不变(1 L)的密闭容器中,加入3 mol PCl3和4 mol Cl2使之发生反应 PCl3(g)+Cl2(g)  PCl5(g),平衡时容器内压强为开始时的6/7。计算并回答 PCl5(g),平衡时容器内压强为开始时的6/7。计算并回答(1) 平衡时,容器内气体密度是开始时的________倍,气体平均相对分子质量是开始时的________倍。 (2)保持同一反应温度,若将起始物改为a mol PCl3,b mol Cl2,c mol PCl5。欲使平衡时PCl5的体积分数为1/6,则a,b,c满足的关系为_________,_________。欲使开始时反应向逆方向进行,则a的取值范围为 _______, b的取值范围为__________,c的取值范围为________。 (3) 保持同一反应温度,若将起始物改为3 mol PCl3,3 mol Cl2,达到平衡时PCl3的转化率为________(百分数表示,保留一位小数;已知:  ) ) |