250 ℃、1.01×105 Pa时,反应 2N2O5(g)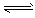 4NO2(g)+O2(g) △H=+56.76 kJ/mol,该反应自发进行的原因是 4NO2(g)+O2(g) △H=+56.76 kJ/mol,该反应自发进行的原因是 |
|
[ ] |
A.是吸热反应
B.是放热反应
C.是熵减少的反应
D.熵增大效应大于能量效应 |
根据n多题专家分析,试题“250℃、1.01×105Pa时,反应2N2O5(g)4NO2(g)+O2(g)△H=+56.76kJ/mol,该反应自发进行的原因是[]A.是吸热反应B.是放热反应C.是熵减少的反应D.熵增大效应大于能量效应…”主要考查了你对 【化学反应进行的方向】 等知识点的理解和应用能力。关于这些知识点的“档案”,你可以点击相应的链接进行查看和学习。
与“250℃、1.01×105Pa时,反应2N2O5(g)4NO2(g)+O2(g)△H=+56.76kJ/mol,该反应自发进行的原因是[]A.是吸热反应B.是放热反应C.是熵减少的反应D.熵增大效应大于能量效应”考查相似的试题有:

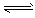 4NO2(g)+O2(g) △H=+56.76 kJ/mol,该反应自发进行的原因是
4NO2(g)+O2(g) △H=+56.76 kJ/mol,该反应自发进行的原因是