氢氧两种元素形成的常见物质有H
2O与H
2O
2,在一定条件下均可分解。
(1)已知:
化学键
| 断开1mol化学键所需的能量(kJ)
|
H—H
| 436
|
O—H
| 463
|
O=O
| 498
|
①H
2O的电子式是
。
②H
2O(g)分解的热化学方程式是
。
③11.2 L(标准状况)的H
2完全燃烧,生成气态水,放出
kJ的热量。
(2)某同学以H
2O
2分解为例,探究浓度与溶液酸碱性对反应速率的影响。常温下,按照如表所示的方案完成实验。
实验编号
| 反应物
| 催化剂
|
a
| 50 mL 5% H2O2溶液
|
| 1 mL 0.1 mol·L-1 FeCl3溶液
|
b
| 50 mL 5% H2O2溶液
| 少量浓盐酸
| 1 mL 0.1 mol·L-1 FeCl3溶液
|
c
| 50 mL 5% H2O2溶液
| 少量浓NaOH溶液
| 1 mL 0.1 mol·L-1 FeCl3溶液
|
d
| 50 mL 5% H2O2溶液
|
| MnO2
|
①测得实验a、b、c中生成氧气的体积随时间变化的关系如图1所示。
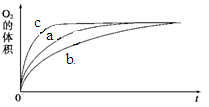

图1 图2
由该图能够得出的实验结论是_________。
②测得实验d在标准状况下放出氧气的体积随时间变化的关系如图2所示。解释反应速率变化的原因:
。


